多部门支持利好政策频出 儿童用药难题引关注
长期以来,儿童专用药供给无法满足临床需求,儿童用药一直存在“用药靠掰、剂量靠猜”难题。近年来,因滥用、错用成人药而导致儿童发生不良反应甚至危及生命的案例增多。解决儿童专用药不足问题,需要从药物研发、生产上发力。然而,对于药品企业来说,一方面,儿童群体的特殊性导致儿童药品研发难度大、盈利难;另一方面,儿童临床试验风险高,志愿者难招募,药物研发缺少数据支撑。
面对日渐增长的儿童用药需求,多部门发布利好政策,促进儿童药研发创新,以顶层设计守护儿童用药安全、可及。
舆情走势及关键节点
以2020年1月1日—2021年6月3日为监测时间段,“儿童用药”相关信息媒体关注度和网民关注度均在2020年8月达到顶峰(见图)。
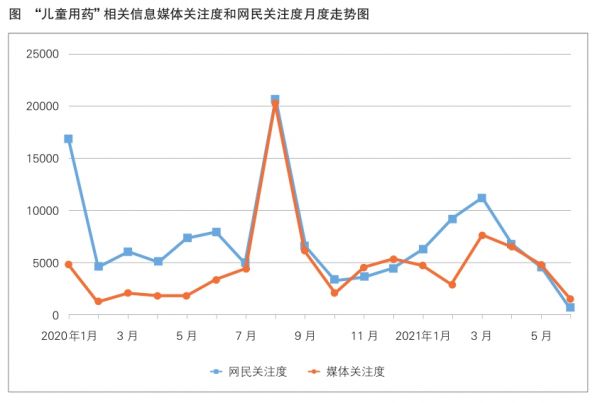
儿童专用药不足引关注
专用药不专,分药成难题
2019年12月3日,《经济参考报》刊发《“专用药不专”?三大短板加剧儿童药匮乏》称,儿童药匮乏是我国医药领域的老问题,三个突出短板加剧儿童药匮乏现状。一是缺乏专用剂型;二是缺乏治疗标准;三是缺乏儿童用药疗效和安全性等信息,儿童药研发难、上市难,药物疗效和安全性难以在儿童人群中验证。
2021年5月11日,微信公众号“医学界”发布的《5岁儿童服药后昏迷:中国儿童药困局》称,现在市场上出现了切药器、带刻度喂药器、药品研磨器等产品,一些家长使用其为孩子分药,这存在很多未知风险。药片分劈、片剂磨粉、粉末溶液化等手工操作很难保证准确和均匀。同时,自行分药而忽视医嘱也带来儿童用药风险。
针对解决“分药”问题,主要有两方面建议。一是建议由儿科医生、药剂师等专业人士分药。如上述《5岁儿童服药后昏迷:中国儿童药困局》引用专家观点,呼吁允许儿科医院收取药品分剂量调配相关药事服务费,激励药师提供更高质量的药品分剂量服务。对于儿科分剂量需求大的药品,鼓励制药企业积极研究分剂量的方法和适宜性,并在药品说明书中添加相应信息。同时,临床工作者应积极探索分剂量对药物溶出度、稳定性等的影响,对分剂量后药物体内处置过程改变、药动-药效学变化以及相应临床风险展开研究。健康报网发布的《医院为患儿“掰药”值得鼓励》称,由医院“掰药”,可在很大程度上缓解家长“猜不准、分不匀”问题。医院可在门诊开通药品分包窗口,为儿童提供分药服务。二是呼吁研发便于分装或儿童专用剂型。如北京日报客户端发布的《剂量靠猜,分药靠掰!难坏家长的儿童用药剂量如何保障?》称,在儿童用药研发上,应在现有药物基础上生产更多便于分装和使用的剂型,如液体剂型、颗粒剂型等,同时提供适合儿童使用的规格,如微型片剂。
成人药儿童用,药物滥用存风险
2021年5月19日,微信公众号“八点健闻”发布的《药监局终于出手!儿童感冒用药的黑历史能否被终结?》称,在美国,2岁以下儿童被禁用的复方抗感冒药,在国内却冠以“小儿”之名,成为年销额数亿元的“大品种”。退热药“尼美舒利”和复方抗感冒药“优卡丹”都曾引发儿童不良反应。
2021年1月8日,《中国医药报》刊发的《10类药物,儿童谨慎使用》称,一些成人可以正常使用的药物,对于处于生长发育特殊时期的儿童来说,可能需要禁用或慎用,如抗菌药物、退热药物、驱虫药、抑酸剂、抗过敏药、止泻药、胃动力药、神经系统药物、镇静催眠药和中药。
家长擅自买药,儿童用药藏隐患
家长热衷海淘的儿童药品并非都安全。2020年10月19日,央视《天下财经》栏目播出的《日本人气儿童感冒糖浆被召回约775万瓶》称,网红感冒药池田模范堂的“面包超人儿童感冒糖浆”在日本被大规模召回,预计数量高达775万瓶。值得注意的是,该企业的“面包超人咳嗽药水”在2017年曾被央视曝光或含我国儿童禁用药成分。中国网、海外网、《北京商报》等媒体转载报道了相关信息。在微博平台上,@凤凰网财经、@21世纪经济报道等也关注该事件。网民认为不应迷信国外人气药品。
儿童罕见病用药被忽视
2020年5月25日,界面新闻发布的《不能“罕治”!两会提案:建议将儿童罕见病用药纳入医保》称,全国人大代表孙伟建议把儿童罕见病用药纳入医保。我国患有罕见病的儿童数量不少,但社会对此关注不多。孙伟代表提出,应做好儿童罕见病诊疗预防工作,逐步把儿童罕见病用药纳入医保。
儿童专用药研发投入多要求高
2020年12月10日,微信公众号“艾美达行业研究”发布的《“儿童药市场”为何呈现出虚假的繁荣?》称,近几年,我国儿童药市场规模快速增长,但儿童药的品种、生产企业却寥寥无几。儿童药生产以小批量、多批次为主,且工艺较复杂,部分儿童药的生产成本比成人药高出10%以上。再加上适用人群有限、价格优势不足,所以虽然儿童药市场潜力巨大,但企业研发生产动力不足。
2021年5月6日,微信公众号“趣学术”发布文章称,企业必须针对儿童生理及心理特点进行专业研发,带来额外研发支出。同时,儿童药生产工艺复杂,推高了生产成本。此外,政府有关部门为防止不合理剂型、奇特剂型抬高药价,在招标时同一药品尽量减少规格和剂型,可儿童药恰恰需要剂型创新,很多儿童药因此落标,也导致儿童药生产企业数量少。
2021年5月20日,微信公众号“人民日报评论”发布的《“剂量靠猜、分药靠掰”,儿童用药如何更精准?》称,不同于成人药物,儿童药物面对的人群数量较少,市场需求远不如成人药物,但研发投入多、要求高。同时,受限于家长让儿童参与临床试验的意愿,儿童药物开展临床试验较难,收集数据难度更大。由于儿童发病往往具有时间短、进程快的特点,对临床试验基地的要求更高、更细致。高投入、高要求、市场规模小,让很多制药企业望而却步。发展完善儿童药物研发、临床试验、供应、使用、支付等体系,仍需要时间。
儿童药研发利好政策频出
近年来,国家药监局、国家卫生健康委、国家医保局等多部门陆续出台多项政策措施,鼓励儿童药物研发、生产、使用。
2020年3月30日,国家市场监管总局发布新修订《药品注册管理办法》《药品生产监督管理办法》,将临床急需的短缺药、儿童用药、罕见病用药等纳入加快上市注册范围。2020年7月发布的《国家卫生健康委办公厅关于加强儿童抗菌药物临床应用监测和细菌耐药监测工作的通知》明确,全国设置儿科诊疗科目的二级及以上医疗机构要全部纳入全国抗菌药物临床应用监测网,进行临床应用数据监测和上报工作。2020年8月,国家药监局药品审评中心(以下简称药审中心)发布《真实世界研究支持儿童药物研发与审评的技术指导原则(试行)》,明确了现阶段真实世界研究支持我国儿童药物研发时的常见情形及关注点,并给出案例及说明。2020年12月,药审中心发布《儿童用药(化学药品)药学开发指导原则(试行)》《儿科用药临床药理学研究技术指导原则》,为儿童用药药学开发提供研发思路和技术指导,进一步明确儿科用药临床药理学研究技术要求。2021年4月、5月,药审中心分别就《儿童用化学药品改良型新药临床试验技术指导原则(征求意见稿)》《化学药品和治疗用生物制品说明书中儿童用药相关信息撰写的技术指导原则(征求意见稿)》公开征求意见,进一步加强儿童用药技术指导。
2020年以来,国家药监局多次发布公告、通知,对部分涉儿童药品进行注销或要求修订药品说明书中涉及儿童的部分,涉及的药品类型包括退热、抗肿瘤、精神科药品等。同时,将创新儿童药品纳入优先审评通道。《中国医药报》刊发的《全力破解儿童用药短缺难题》显示,截至今年5月底,通过优先审评通道获批上市的儿童用药累计达32个,2021年以来已有12个儿童用药获批上市,完成数量及审评速度均有明显提升。2021年5月31日,药审中心网站正式开通“儿童用药专栏”。栏目汇集儿童用药领域的政策法规、技术指南等信息,未来将成为企业、医生、公众了解国家儿童用药政策法规、把握研发技术要求、与药监部门互动沟通的重要窗口。
另外,在医保目录、产业组织方面对儿童用药也有利好。2020年国家医保谈判结果显示,共收录7种儿科用药,包括小儿清热宁颗粒、小儿法罗培南颗粒、小儿牛黄清心散、小儿荆杏止咳颗粒、安儿宁颗粒等,多为中成药品种。这7款药品均充分考虑药品安全性与有效性,规格和剂型较符合儿童特点,对儿童用量也有明确规定。2020年10月24日,中国儿童药物研发和产业化联盟启动大会在北京召开,工业和信息化部、国家卫生健康委联合支持成立儿童药物研发和产业化联盟。联盟集中医药行业优势资源,密切统筹研发、生产和临床需求,推动多学科、跨领域合作,促进儿童用药产业发展。(中国健康传媒集团舆情监测中心 占妮)
责任编辑:露儿
-
一批药被查 涉维C银翘片、阿胶…
一批药被查 涉维C银翘片、阿胶…...
-
高值耗材最高降价80% 涉雅培、波科、贝朗…
8月1日,云南省曲靖市举行高值医用耗材联盟带量集中采购第一批次中选产品企业签约仪式。...
-
国家指令 整治所有医院回扣 暗访组出发
日前,国家卫健委发布了《2020年医疗行业作风建设工作专项行动方案》,这次方案的重点就是规范医疗机构及其从业人员行为,印发给各省、自治区、直辖市及新疆生产建设兵团卫生健康委,开始组织实施。...
-
医药代表系统学习产品知识的十个步骤
每个刚入行的医药代表初期都会接受公司大量培训,产品知识培训更是重中之重,不仅培训而且还要考试。...
-
“3+6”医用耗材带量采购,价格信息公布
吉林省政府采购中心消息发布《京津冀及黑吉辽蒙晋鲁医用耗材(人工晶体类)联合带量采购文件(LH-HD2020-1)》(下称《采购文件》),公布人工晶体类耗材的具体采购品种、申报价格等信息。 ...
-
首轮价格降幅低于42% 医疗器械企业直接淘汰
首轮价格降幅低于42% 医疗器械企业直接淘汰...
-
Q1最惨淡的两大药品领域,代表都离职了!
中国虽然是世界上最先控制住疫情的国家,但随着全球疫情的爆发,输入病例不断上升,加上中国本土还有不少无症状感染患者,这使得中国经济无法完全恢复正常。...
-
某些药企又要开启新一轮裁员了
做代表难,今年更加难。除了国家级的带量采购,省级也有带量采购,感觉就像是夹缝中求生存。...
-
两家外企大裁员,患教专员全部解散!
两家外企大裁员,患教专员全部解散!...
-
执业药师挂证,面临终生逐出行业的巨大风险
执业药师挂证,面临终生逐出行业的巨大风险...
-
虚开发票2.5亿,涉多家药械企业(附目录)
近日,国家税务总局马鞍山市税务局发布的《重大税收违法案件信息公告2020年3月》显示,51家企业涉嫌虚开发票,其中24家是药械企业或相关资讯、服务企业。...
-
91家药企收入公开:以岭、科伦、康恩贝…
突如其来的新冠肺炎疫情,对中国的冲击力和冲击面都超过了2003年的非典,对中国经济乃至世界经济也产生了不可避免的影响,也严重扰乱了正常的经济运行节奏。...





















