临床试验默许制开闸9个月,恒瑞、石药等布局最快!
自2018年11月5日国家药品监督管理局药品审评中心公布首批临床试验默示许可公示8个受理号,至2019年4月27日,咸达数据V3.5发现,国家药品监督管理局药品审评中心已公布577个受理号默认批准临床。这意味着药物临床试验审评审批“默许制”的落地已常态化。
2018年7月27日,国家药品监督管理局发布了《关于调整药物临床试验审评审批程序的公告》,标志着我国药物临床试验审评审批制度正式由审批制变为到期默认制。《公告》明确,在我国申报药物临床试验的,自申请受理并缴费之日起60日内,申请人未收到国家药品监督管理局药品审评中心否定或质疑意见的,可按照提交的方案开展药物临床试验。
那么,哪些产品进入临床试验默许?从中透露出哪些研发动向?
注册分类
化学药 PK 生物药 PK 中药
577个受理号中,属于化学药的有356个,生物制品有206个(其中,预防用生物制品21个,治疗用生物制品185个),中药15个。
化学药:新药申报活跃
化学药申报中,属于国内新药申报的有146个,进口申报的有135个,补充申请的有40个,仿制药申报的有35个。
国内新药中,新1类新药(境内外均未上市的创新药)129个,是最主要的申报分类。
进口药方面,进口新药新1类的申请受理号55个,5.1类(境外上市的原研药品申请在境内上市)34个,5.2类(境外上市的非原研药品申请在境内上市)23个。
化学药仿制药方面,新3类(仿制境外上市但境内未上市原研药品的药品)18个,新4类(仿制境内已上市原研药品的药品)14个,旧6类(已有国家药品标准的原料药或制剂)3个。
化学仿制药:吸入剂最受青睐
值得注意的是,新注册分类5.2类也可以临床默许了。仿制药此前启动的BE备案制只适用于国内仿制药新3类和新4类,进口仿制药5.2类申报仍需要报临床。因此,临床试验默许制实施将加快进口仿制药在中国上市。除了印度企业和日本企业,辉瑞和诺华都在积极将自己的仿制药业务引进中国。
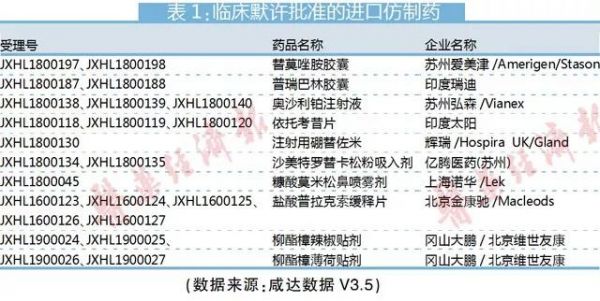
仿制药新3类最多产品被临床默认批准的类别是吸入剂,如吸入用色甘酸钠溶液/色甘酸钠吸入溶液,富马酸福莫特罗吸入溶液和色甘酸钠吸入溶液。
新4类则是吸入类和复杂注射剂,吸入类的产品有乌美溴铵维兰特罗粉吸入剂、沙美特罗替卡松吸入气雾剂、吸入用布地奈德混悬液/布地奈德吸入混悬液、丙酸氟替卡松鼻喷雾剂、吸入用硫酸沙丁胺醇溶液;复杂注射剂则有棕榈酸帕利哌酮注射液(3个月)、注射用醋酸亮丙瑞林微球和美洛昔康混悬注射液。
生物药:单抗类占比近五成
治疗用生物制品185个受理号中,有36个是补充申请,76个是进口申请,剩下的73个全是国内新药申请(其中1类新药44个)。185个受理号中,有82个是单抗类药品,占比为44%。
预防用生物制品申报较多的疫苗是冻干人用狂犬病疫苗(Vero细胞)和四价流感病毒裂解疫苗。
中药:颗粒剂申报最多
中药的15个批文中,有10个是新药申请,5个是补充申请。中药新药申请中,1个是新4类,1个是6.1类(未在国内上市销售的中药、天然药物复方制剂)。中药颗粒剂是最多申报的剂型。新疆维吾尔自治区药物研究所共有5个产品被临床默认许可。
企业布局
国内标杆PK进口标杆
国内企业
No.1、恒瑞 主要领域:涉及面广,肿瘤为主
恒瑞是国内企业最多产品被批准临床默许的,获批的产品有15个,包括氟唑帕利胶囊、SHR2285片(预防或治疗动静脉血栓,以及降低介入治疗或体外循环引起的血栓栓塞风险)、罂粟乙碘油注射液、美洛昔康混悬注射液、SHR-2042(2型糖尿病及肥胖症的治疗)、SHR9549片(ER阳性、HER2阴性的乳腺癌的治疗)、SHR2150胶囊(晚期恶性肿瘤的治疗)、盐酸右美托咪定鼻喷雾剂、注射用卡瑞利珠单抗、SHR-1222注射液(治疗骨质疏松症)、SHR0302片(治疗克罗恩病)、DDO-3055片(慢性肾病所致贫血包括透析和非透析的治疗)、甲磺酸阿帕替尼片、SHR3680片(治疗转移性去势抵抗性前列腺癌,mCRPC)、注射用SHR-A1201(治疗HER2阳性的转移性乳腺癌患者),对应获批受理号共31个。
由此可见,恒瑞的新药研发涉及领域较多,其中肿瘤仍是其研发的主要方向。
No.2、东阳光、石药 东阳光:治疗领域分散 石药:涉及面广,肿瘤为主
东阳光和石药各共有11个受理号,并列第二。
东阳光主要产品有HEC110114片(与其它直接抗病毒药物联用,治疗慢性丙型肝炎病毒感染症)、HEC53856胶囊(治疗慢性肾脏病相关的贫血,包括透析和非透析病人)、HEC113995PA·H2O片(抑郁症)、重组抗TNF-α全人源单抗注射液、利拉鲁肽注射液。治疗领域比较分散。
石药集团研发的产品有SYHA136片(治疗髋关节或膝关节择期置换术的成年患者、预防静脉血栓栓塞事件VTE)、SYHA1803胶囊(治疗肝内胆管癌、尿路上皮细胞癌)、SYHA1402片(治疗糖尿病周围神经病变)、注射用紫杉醇阳离子脂质体和注射用紫杉醇(白蛋白结合型)。
注射用紫杉醇(白蛋白结合型)石药已经通过一致性评价,2019年补充申请被批准临床默认。从CDE公布的适应症来看,2019年申请的适应症为“适用于治疗联合化疗失败的转移性乳腺癌或辅助化疗后6个月内复发的乳腺癌。除非有临床禁忌症,既往化疗中应包括一种蒽环类抗癌药”。与一致性评价获批的适应症一致。
No.4、贝达 主要领域:坚持肿瘤药方向
贝达药业及其控股子公司卡南吉医药科技也有10个受理号获得临床默认批准,包括MRX2843片(治疗AML、ALL等血液瘤以及实体瘤)、BPI-17509片(肝内胆管癌、膀胱癌和肺鳞癌等FGFR基因变异等实体瘤的治疗)、BPI-23314片(治疗恶性血液系统肿瘤,包括急性髓系白血病、非霍奇金淋巴瘤和多发性骨髓瘤)、CM082片(治疗既往未经治疗的局部进展或转移性黏膜黑色素瘤)。
由此可见,贝达自埃克替尼成功案例后,坚持抗肿瘤的战略方向。
外企
No.1、杨森 主要领域:肿瘤、免疫
进口厂家方面,杨森共17个受理号获得临床默认批准,乌司奴单抗注射液、Pimodivir速释薄膜包衣片(用于急性甲型流感住院患者和高危门诊患者)、人源抗CD38单抗(Daratumumab)皮下注射液(治疗淀粉样变性和高危冒烟型多发性骨髓瘤)、Guselkumab注射液(治疗中重度活动性克罗恩病)、JNJ-61186372注射液(治疗局部晚期或转移性非小细胞肺癌(NSCLC))、马昔腾坦片和阿帕鲁胺片。主要方向是肿瘤和免疫系统用药。
No.2、诺华 主要领域:肿瘤、免疫、抗过敏
诺华制药共14个受理号获得临床默认批准,包括ACZ885(治疗局部晚期或转移性非鳞状及鳞状非小细胞肺癌)、CFZ533(治疗系统性红斑狼疮)、VAY736(治疗系统性红斑狼疮)、曲美替尼片、CJM112(治疗低IgE以及低循环嗜酸性粒细胞水平的中至重度难控制性哮喘)、糠酸莫米松鼻喷雾剂、达拉非尼胶囊和PKC412软胶囊。PKC412软胶囊治疗FLT3突变阳性(FLT3-MP)和FLT3突变阴性(FLT3-MN)急性髓系白血病(AML)。
No.3、阿斯利康 主要领域:肿瘤联合疗法
阿斯利康有12个受理号获得临床默认批准,分别是Durvalumab(联合治疗肝细胞癌、Ⅰ~Ⅲ期局限期小细胞肺癌、不可切除性局部晚期或转移性尿路上皮癌、FIGOⅠB2期至ⅣA期宫颈癌)、Tremelimumab(联合治疗Ⅰ~Ⅲ期局限期小细胞肺癌、不可切除性局部晚期或转移性尿路上皮癌)、Acalabrutinib胶囊(治疗慢性淋巴细胞性白血病CLL)、奥拉帕利片、Pelareorep注射液(治疗晚期/转移性乳腺癌)和替格瑞洛分散片。
阿斯利康申报的临床基本都是联合疗法,例如奥拉帕利在2018年作为首个PARP抑制剂已经在国内上市,适应症为用于治疗BRCA胚系突变铂敏感复发性卵巢癌患者。临床默认对应的受理号是2018年申报的,申报的适应症为奥拉帕利与阿比特龙和强的松合并使用,用于转移性去势抵抗性前列腺癌患者的治疗。
展望>>>
抗肿瘤依然是国内临床研发的热点,577个受理号中,与肿瘤相关的受理号有203个。此外,糖尿病相关的受理号68个,疼痛相关的受理号38个,也是研发热点。
临床试验默认制会促进新药研发和进口仿制药申报增加,新药联合疗法的申报也会增加,国内新药有望和全球同步上市。
责任编辑:露儿
-
一批药被查 涉维C银翘片、阿胶…
一批药被查 涉维C银翘片、阿胶…...
-
高值耗材最高降价80% 涉雅培、波科、贝朗…
8月1日,云南省曲靖市举行高值医用耗材联盟带量集中采购第一批次中选产品企业签约仪式。...
-
国家指令 整治所有医院回扣 暗访组出发
日前,国家卫健委发布了《2020年医疗行业作风建设工作专项行动方案》,这次方案的重点就是规范医疗机构及其从业人员行为,印发给各省、自治区、直辖市及新疆生产建设兵团卫生健康委,开始组织实施。...
-
医药代表系统学习产品知识的十个步骤
每个刚入行的医药代表初期都会接受公司大量培训,产品知识培训更是重中之重,不仅培训而且还要考试。...
-
“3+6”医用耗材带量采购,价格信息公布
吉林省政府采购中心消息发布《京津冀及黑吉辽蒙晋鲁医用耗材(人工晶体类)联合带量采购文件(LH-HD2020-1)》(下称《采购文件》),公布人工晶体类耗材的具体采购品种、申报价格等信息。 ...
-
首轮价格降幅低于42% 医疗器械企业直接淘汰
首轮价格降幅低于42% 医疗器械企业直接淘汰...
-
Q1最惨淡的两大药品领域,代表都离职了!
中国虽然是世界上最先控制住疫情的国家,但随着全球疫情的爆发,输入病例不断上升,加上中国本土还有不少无症状感染患者,这使得中国经济无法完全恢复正常。...
-
某些药企又要开启新一轮裁员了
做代表难,今年更加难。除了国家级的带量采购,省级也有带量采购,感觉就像是夹缝中求生存。...
-
两家外企大裁员,患教专员全部解散!
两家外企大裁员,患教专员全部解散!...
-
执业药师挂证,面临终生逐出行业的巨大风险
执业药师挂证,面临终生逐出行业的巨大风险...
-
虚开发票2.5亿,涉多家药械企业(附目录)
近日,国家税务总局马鞍山市税务局发布的《重大税收违法案件信息公告2020年3月》显示,51家企业涉嫌虚开发票,其中24家是药械企业或相关资讯、服务企业。...
-
91家药企收入公开:以岭、科伦、康恩贝…
突如其来的新冠肺炎疫情,对中国的冲击力和冲击面都超过了2003年的非典,对中国经济乃至世界经济也产生了不可避免的影响,也严重扰乱了正常的经济运行节奏。...





















