多个重磅药面临专利悬崖,新一轮大降价,开始了!
多个重磅药面临专利悬崖,新一轮大降价,开始了!
3月4日,国外医药网站FiercePharma发布了一份2019年可能面临专利挑战风险的十大药物清单。

根据报道,在2019年有多款重磅专利药将失去市场独占权,面临仿制药的竞争。这些专利药即将遭遇“专利悬崖”,随着便宜的仿制药涌入,毫无悬念,这些专利药的价格将大幅下降。
其中包括来自辉瑞的Lyrica(乐瑞卡)、葛兰素史克的Advair(舒利迭)、罗氏的Rituxan(美罗华)、吉利德的Harvoni(夏帆宁)及许多其他药物,这些药物将在今年面临或预期面临仿制药竞争。
根据清单,我们可以发现,很多我们熟悉的产品,包括辉瑞的Lyrica(乐瑞卡)、葛兰素史克的Advair(舒利迭)、罗氏的Rituxan(美罗华)、吉利德的Harvoni(夏帆宁)等。
 (来源:FiercePharma) 其中,Herceptin(赫赛汀)、Avastin(安维汀)、Rituxan(美罗华)均是罗氏的王牌产品。根据罗氏2018年业绩报告,上述3款产品的全球销售额分别高达69.82亿、68.49亿、67.52亿瑞士法郎,美国市场分别为29.08亿、29.04亿、42.9亿瑞士法郎。
(来源:FiercePharma) 其中,Herceptin(赫赛汀)、Avastin(安维汀)、Rituxan(美罗华)均是罗氏的王牌产品。根据罗氏2018年业绩报告,上述3款产品的全球销售额分别高达69.82亿、68.49亿、67.52亿瑞士法郎,美国市场分别为29.08亿、29.04亿、42.9亿瑞士法郎。
这三大王牌产品的专利到期,无疑是各药企接下来仿制的重要目标。
此外,辉瑞的Lyrica(乐瑞卡)和葛兰素史克的Advair(舒利迭)也是家喻户晓的品牌药,这2个药再次出现在了2019年的清单中。
随着越来越多重磅产品即将面临专利悬崖,全球制药巨头们无疑将迎来严峻的挑战。未来,这些重磅药的后续市场将会怎样变化,是业界共同关注的。
以下是2019年可能面临专利挑战风险的十大药物的概况:

(图片来源:新浪医药) Rituxan(美罗华,利妥昔单抗)
美罗华由罗氏销售,2017年全球销售额为79亿美元,其中美国市场销售额44.1亿美元,该药美国市场专利保护截止日期为2018年年中至年底。
美罗华于1997年首次获批上市,目前获批适应症包括多种血液癌症(如非霍奇金淋巴瘤和慢性淋巴细胞白血病)和免疫性疾病(如类风湿性关节炎)。
由于预期专利保护期满后生物仿制药公司竞争的加剧,罗氏Rituxan的销售额将呈现下滑。目前,山德士、梯瓦、Celltrion均已向美国FDA提交了各自的利妥昔单抗生物仿制药申请。在欧洲,来自山德士和Celltrion公司的利妥昔单抗生物仿制药已获批准。
2月25,国家药监局宣布复宏汉霖旗下利妥昔单抗在2月22日获得上市批文。这是我国首个生物类似药,罗氏的美罗华在中国第一次遇到竞争对手。此外,目前利妥昔单抗类似药申报的国内企业已有十几家,除了复宏汉霖,另有信达生物、神州细胞工程、喜康生物、海正药业4家公司的产品进入临床Ⅲ期。
据米内网数据显示,2018年美罗华在中国医院市场的销售额高达29.42亿元,且近几年都保持比较稳定的市场增速。随着美罗华专利到期,国内仿制药的获批,将会对其市场带来一定的冲击。
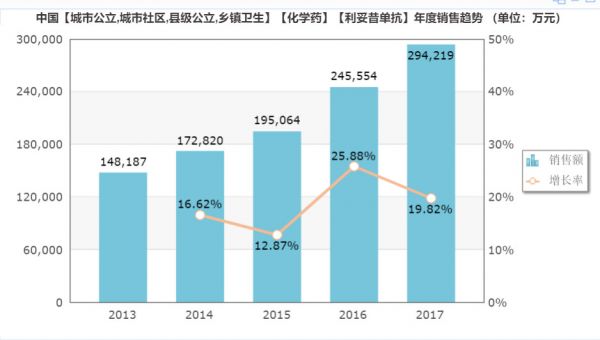 (数据来源:米内网)
(数据来源:米内网)
Herceptin(赫赛汀,注射用曲妥珠单抗)
赫赛汀是由瑞士罗氏公司研发的一种重组DNA衍生的人源化单克隆抗体,适应症为转移性乳腺癌,可有效抑制肿瘤细胞的生长。1998年9月首先被美国FDA批准上市,2002年获准进口我国。
根据罗氏财报显示,赫赛汀2018年全球销售额为69.29亿美元,同比增长1%。罗氏在财报中表示,增长动力主要来自美国和中国市场,而在欧洲和日本市场,由于生物类似药的竞争,赫赛汀的销售额同比下降16%。
而在中国市场却完全不一样。在2017年7月国家将赫赛汀进医保前,赫赛汀单支售价2.45万元,患者一年需要使用使用14支以上,全年使用费用约40万元。然而在进医保后,赫赛汀单支价格降为7600元,普通家庭的患者也能支付得起,一时间引发了销量暴增。
米内网数据显示,2018年赫赛汀在中国医院市场的销售额高达26.22亿元,市场增速高达37.06%。
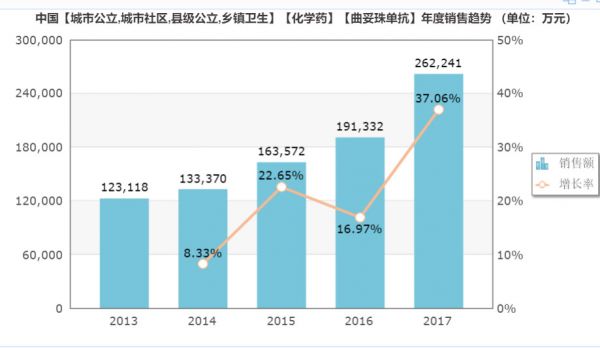 (数据来源:米内网)
(数据来源:米内网)
赫赛汀在欧盟的专利已于2014年7月到期,美国专利也将于2019年6月到期。目前,国内外医药企业纷纷加入到其生物类似药的研发中。接下来,随着专利到期,仿制药获批,赫赛汀的销量将会受一定影响。
Avastin(安维汀,贝伐珠单抗注射液)
安维汀是罗氏的王牌产品之一。2013年销售额为71.06亿美元,比2012年增长8.5%。欧洲的专利到期时间是2018年,美国则是2019年。
不过,这个产品面临的市场挑战,已经显现。该药物在欧盟即将面临安进/艾尔健最近许可的生物类似药 Mvasi 的激烈竞争,Mvasi是欧盟批准的首个贝伐单抗仿制版本药物。
在中国,CDE近期正式受理了信达的仿制品的上市申请。
据米内网数据显示,2018年安维汀在中国医院市场的销售额高达15.82亿元,市场增速高达40.33%,且市场增速稳步逐年上涨。随着安维汀专利到期,国内仿制药的获批,将会对其市场带来一定的冲击。
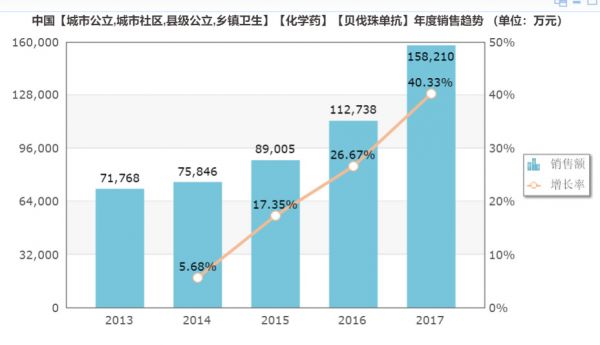 (数据来源:米内网)
(数据来源:米内网)
Advair(舒利迭,沙美特罗替卡松)
舒利迭由葛兰素制药公司开发并于1998年获得FDA批准,素有哮喘药“金标准”之称,随后在美国和欧盟多个国家用于临床。
虽然2010年舒利迭在美国市场就已经失去专利保护,但其给药装置的专利保护期至2016年。因此,该产品很难被其他企业仿制。在经历数次推延之后,舒利迭最终也将面临仿制药的竞争。今年2月,迈兰的Godot获得FDA批准上市,这意味着,舒利迭迎来了新一波仿制药冲击。
米内网数据显示,2018年舒利迭在中国医院市场的销售额为14.2亿元,近几年市场增长比较平缓,基本处于停滞状态。接下来,随着仿制药逐渐获批,舒利迭的销量将会进一步受到影响。
 (数据来源:米内网)
(数据来源:米内网)
Lyrica(乐瑞卡,普瑞巴林)
乐瑞卡是由辉瑞销售,全球最畅销的镇痛药,2017年销售额为51亿美元,其中美国市场销售额为34.6亿美元。
根据FiercePharma报道,乐瑞卡原本是在去年底失去专利保护,但一项儿科适应症将其专利保护延长了6个月时间。为了延长独占期,辉瑞此前也向美国FDA提交了每日一次的延长释放版乐瑞卡,用于治疗带状疱疹或糖尿病周围神经病变引起的疼痛。
据米内网数据,2018年乐瑞卡在中国医院市场的销售额为14.2亿元,市场增速高达122.81%。可见,对于该品种的市场需求正在不断加大。
 (数据来源:米内网)
(数据来源:米内网)
责任编辑:露儿
-
一批药被查 涉维C银翘片、阿胶…
一批药被查 涉维C银翘片、阿胶…...
-
高值耗材最高降价80% 涉雅培、波科、贝朗…
8月1日,云南省曲靖市举行高值医用耗材联盟带量集中采购第一批次中选产品企业签约仪式。...
-
国家指令 整治所有医院回扣 暗访组出发
日前,国家卫健委发布了《2020年医疗行业作风建设工作专项行动方案》,这次方案的重点就是规范医疗机构及其从业人员行为,印发给各省、自治区、直辖市及新疆生产建设兵团卫生健康委,开始组织实施。...
-
医药代表系统学习产品知识的十个步骤
每个刚入行的医药代表初期都会接受公司大量培训,产品知识培训更是重中之重,不仅培训而且还要考试。...
-
“3+6”医用耗材带量采购,价格信息公布
吉林省政府采购中心消息发布《京津冀及黑吉辽蒙晋鲁医用耗材(人工晶体类)联合带量采购文件(LH-HD2020-1)》(下称《采购文件》),公布人工晶体类耗材的具体采购品种、申报价格等信息。 ...
-
首轮价格降幅低于42% 医疗器械企业直接淘汰
首轮价格降幅低于42% 医疗器械企业直接淘汰...
-
Q1最惨淡的两大药品领域,代表都离职了!
中国虽然是世界上最先控制住疫情的国家,但随着全球疫情的爆发,输入病例不断上升,加上中国本土还有不少无症状感染患者,这使得中国经济无法完全恢复正常。...
-
某些药企又要开启新一轮裁员了
做代表难,今年更加难。除了国家级的带量采购,省级也有带量采购,感觉就像是夹缝中求生存。...
-
两家外企大裁员,患教专员全部解散!
两家外企大裁员,患教专员全部解散!...
-
执业药师挂证,面临终生逐出行业的巨大风险
执业药师挂证,面临终生逐出行业的巨大风险...
-
虚开发票2.5亿,涉多家药械企业(附目录)
近日,国家税务总局马鞍山市税务局发布的《重大税收违法案件信息公告2020年3月》显示,51家企业涉嫌虚开发票,其中24家是药械企业或相关资讯、服务企业。...
-
91家药企收入公开:以岭、科伦、康恩贝…
突如其来的新冠肺炎疫情,对中国的冲击力和冲击面都超过了2003年的非典,对中国经济乃至世界经济也产生了不可避免的影响,也严重扰乱了正常的经济运行节奏。...





















