“289大限”将至 近200个“三无品种”出局?
7月31日,CDE发布公告称,为加快推进“289品种”一致性评价工作,特对289目录中的国内特有品种进行梳理调研,对这些品种形成评价建议,并向社会公开征求意见。截至目前,距离完成“289品种”一致性评价工作只剩5个月的时间。
据统计,截至2018年7月31日,通过一致性评价的“289品种”只有13个,此外36个品种正在申请一致性评价,其中6个品种有企业通过一致性评价。据米内网数据,“289品种”中仍有近200个品种处于无BE临床试验登记、无一致性评价申请、无通过一致性评价的“三无状态”,2018年底大限将至,这些“三无品种”该何去何从?会被淘汰出局吗?
大限将至,“289品种”仅13个通过一致性评价
2016年5月26日,国家药品监督管理局发布公告:“凡2007年10月1日前批准上市的列入国家基本药物目录(2012年版)的化学药品仿制药口服固体制剂,原则上应在2018年底前完成一致性评价”。在2016年第106号文件中,列出了289个基药品种,按照公告要求,这些品种原则上应在2018年底前完成一致性评价,此即“289大限”。

(来源:国家药品监督管理局官网)
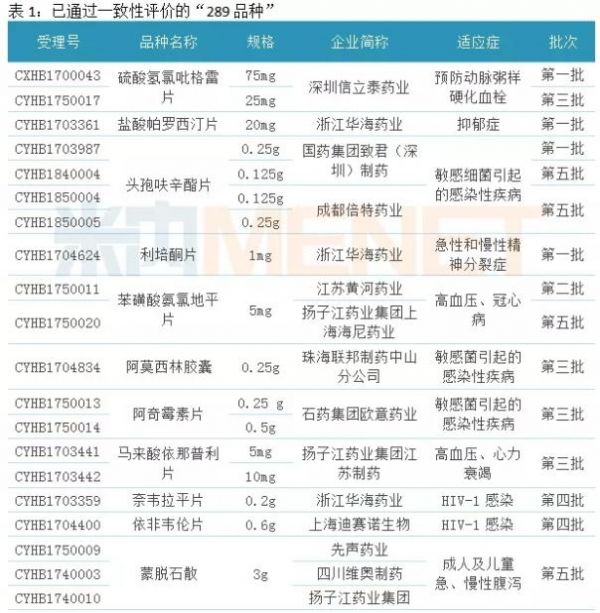
截至目前,国家药品监督管理局共公布5批通过一致性评价的药品名单,涉及31个品种(57个受理号),其中仅有13个品种(24个受理号)为“289品种”。国家药监局发布最后一批通过一致性评价药品名单至今,华润赛科药业的苯磺酸氨氯地平片(受理号CYHB1840005)也审批完成,通过一致性评价。因此,截至2018年7月31日,“289品种”中共有13个品种(25个受理号)通过一致性评价。
硫酸氢氯吡格雷片、头孢呋辛酯片、马来酸依那普利片、阿法骨化醇片等品种所有规格均有企业申报并通过一致性评价,其中头孢呋辛酯片竞争较为激烈,全部品规均有2家企业通过一致性评价;苯磺酸氨氯地平片、蒙脱石散这2个品种单一规格均有3家企业申报并通过一致性评价;在需要进行一致性评价的“289品种”中,阿奇霉素片只有0.25g这一规格需要通过一致性评价,但是石药集团欧意药业申报了0.25g与0.5g两种规格,并且都通过了一致性评价。
从通过“289品种”一致性评价的企业看,浙江华海药业、扬子江药业集团及子公司均有3个品种通过一致性评价,石药集团及子公司有2个品种通过一致性评价。
百亿大品种领跑,36个“289品种”申报一致性评价
据米内网MED中国药品审评数据库2.0数据,截至2018年7月31日,申报一致性评价的205个受理号(不包括已经通过或不批准通过一致性评价的受理号)中,有87个受理号属于“289品种”,涉及品种36个。
(来源:米内网数据库,统计截至2018年7月31日)
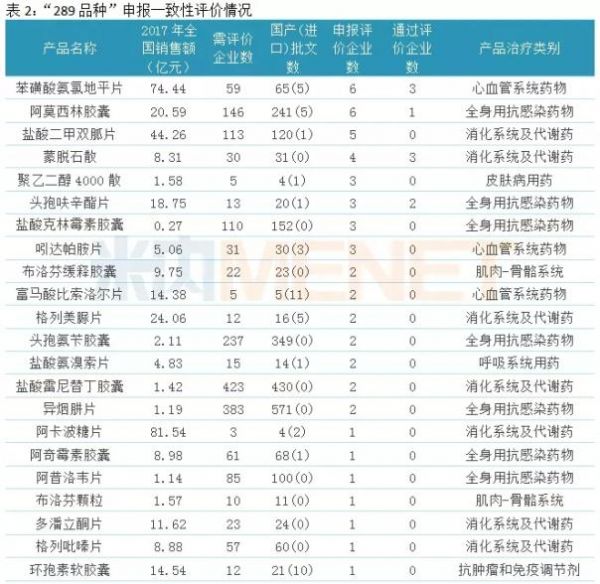
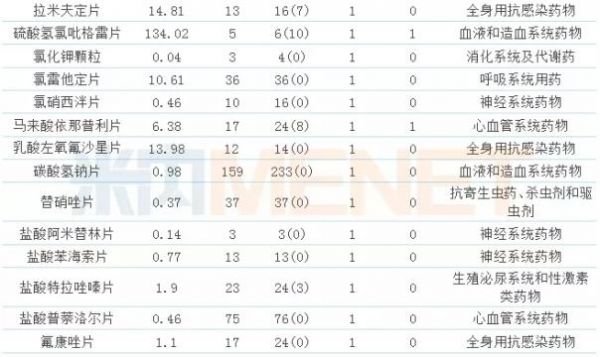
36个申报一致性评价品种中,有10个属于全身用抗感染药物,有8个属于消化系统及代谢药,两大品类产品占据“半壁江山”,据米内网数据,全身用抗感染药物、消化系统及代谢药在2017年中国公立医疗机构终端化学药格局中,分别以19.95%及16.58%的市场份额位居首位与第二位。
从产品2017年全国销售额看,硫酸氢氯吡格雷片是申报一致性评价品种中唯一一个销售额超过百亿的产品;包含百亿大品种在内,超过10亿元的产品共有13个。
从需评价企业数及批文数看,拥有生产批文的企业数超过100家的产品有7个,合计批文总数2102条,而从这些产品在2017年全国销售额看,除了阿莫西林胶囊、盐酸二甲双胍片超过10亿元以外,其余几个产品销售额都较低,拥有383家生产企业,571个药品批文的异烟肼片在2017年全国销售额仅为1.19亿元,这从侧面反映,我国仿制药重复建设、重复申请,市场恶性竞争现象比较严重。
从申报一致性评价企业及数量看,四川科伦药业及子公司申报品种数最多,共有6个;其次是石药集团及子公司,申报品种数达4个;苯磺酸氨氯地平片竞争激烈,除了已经通过一致性评价的3家企业,还有6家企业申请该产品的一致性评价,从承办时间看,上海诺华贸易的苯磺酸氨氯地平片的一致性评价申请已于2017年年底受到承办,目前还处于“已发件”状态。阿莫西林胶囊竞争也较为激烈,共有6家企业申请该产品一致性评价,从承办时间看,石药集团中诺药业(石家庄)的阿莫西林胶囊最早受到承办,但目前还处于“审评审批中”状态。
从通过一致性评价企业数看,苯磺酸氨氯地平片、蒙脱石散已有3家企业通过一致性评价,而头孢呋辛酯片已有2家企业通过一致性评价,只要再有1家企业通过一致性评价,那么在药品集中采购等方面将不再选用未通过一致性评价的品种。
近200个“三无品种”何去何从?延期OR淘汰?
据米内网数据,阿卡波糖胶囊、阿立哌唑片及口崩片、阿莫西林克拉维酸钾片、富马酸喹硫平片、吲达帕胺缓释片、盐酸昂丹司琼片、硝苯地平缓释片(Ⅱ)、缬沙坦胶囊、盐酸倍他司汀片、阿奇霉素颗粒等40多个品种虽然还未有企业提出一致性评价申请,也未有通过一致性评价的企业,但已有企业进行BE试验登记,其中克拉霉素片、奥美拉唑肠溶胶囊等品种登记BE试验企业数是较多的。
分析这些品种,可发现有些品种的BE试验是部分厂家按照新4类仿制药标准登记进行的BE试验,这些品种一旦获批生产亦视同通过一致性评价,如天津力生的吲达帕胺缓释片等。
截至2018年7月31日,“289品种”中有近200个品种目前处于无BE临床试验登记、无一致性评价申请、无已通过一致性评价的“三无”状态,我们将这些品种称为“三无品种”。

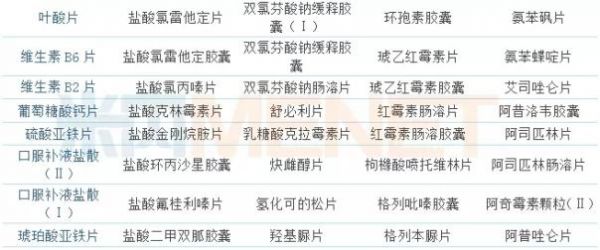
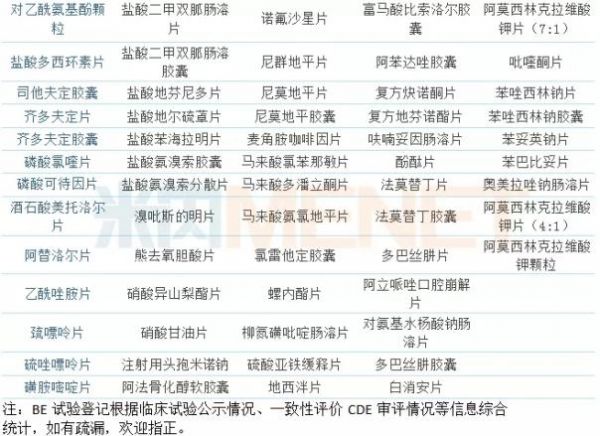
(来源:米内网数据库,统计截至2018年7月31日)
分析这些“三无品种”,19个国内特有品种赫然在列(表中作红色标识的品种),这些国内特有品种市场规模都比较小,多数药品售价较为低廉,生产企业的利润较为微薄,此外这些品种国外没有,无法找到参比制剂,且进行一致性评价所需要的费用可能在几百万到数千万,不少企业都会选择直接放弃,而这也意味着这些国内特有品种可能会退出市场。
对这些品种的一致性评价,CDE在2017年4月提出了具体规定:由企业选择可重新开展临床试验证明其安全有效性,并参照《化学药品仿制药口服固体制剂质量和疗效一致性评价申报资料要求(试行)》提交申请,后续审核通过后视同通过一致性评价;企业未选择重新开展临床试验的,国家药品监督管理局对外公布其缺乏有效性数据,不建议使用。
据7月31日CDE发布的最新通知,国内特有品种较之前增加了3个,共计22个,在对各品种的评价建议中,乳酶生片、复方氢氧化铝片、醋酸泼尼松片等12个品种无需开展临床有效性,盐酸小檗碱片、乳酶生片等5个品种不推荐参比,制霉素片、氢溴酸山莨菪碱片等7个品种开展临床有效性试验,联苯双酯片不建议开展再评价。此外制霉素片、复方氢氧化铝片等6个品种因临床证据不足需要修订说明书。
还有部分“三无品种”属于可豁免或简化人体生物等效性(BE)试验的品种(表中蓝色标识的品种),今年5月底,国家药监局发布了可豁免或简化人体生物等效性(BE)试验的48个品种,包括口服补液盐散、维生素B2及B6片、琥珀酸亚铁片、硫酸亚铁片、氯化钾颗粒等15个品种可豁免人体BE;酒石酸美托洛尔片、盐酸普萘洛尔片、左氧氟沙星片等7个品种自证BCS分类,再申请豁免BE;替硝唑片、利福平胶囊、卡托普利片、吲达帕胺片等13个品种可简化BE。
上述48个品种中,蒙脱石散、卡托普利片已有企业通过一致性评价;异烟肼片、氯化钾颗粒、聚乙二醇4000散、碳酸氢钠片、拉米夫定片、盐酸雷尼替丁胶囊、盐酸特拉唑嗪片、吲达帕胺片、替硝唑片、氟康唑片、盐酸普萘洛尔片等均有企业申报一致性评价;对乙酰氨基酚片、利福平胶囊、甲硝唑片、左氧氟沙星片等均有企业登记BE临床试验。
7月31日,CDE发布了第二批可豁免或简化人体生物等效性(BE)试验的品种,共计15个,包括维生素C泡腾片、聚乙二醇钠钾散等9个品种可豁免BE;甲钴胺片、替莫唑胺片等6个品种自证BCS分类,再申请豁免BE。
此外,有一大部分“三无品种”是“三改”品种,如利福平片、醋酸甲羟孕酮片、联苯双酯滴丸等,这些品种做一致性评价难度大。还有一部分是临床用量很小或因安全性问题被淘汰的品种,如酚酞片等。这两类品种,很少有企业愿意做一致性评价。
但还有一些品种,在临床经常使用且销售额可观,还处于“三无”状态,如注射用头孢米诺钠、阿法骨化醇胶囊及软胶囊,双氯芬酸钠缓释胶囊等,这些产品在2017年中国公立医疗机构终端销售额分别22.7亿元、7.8亿元、5.8亿元,拥有这些产品批文的药企可要加快速度了。
结语
从目前“289品种”一致性评价进程来看,要在这仅剩下的不到半年时间完成全部品种的一致性评价似乎有很大难度,这是否意味着这些未通过一致性评价的品种将遭到淘汰?
据医药经济报报道,近日,“一致性评价在行动暨高质量仿制药推进工作研讨会”召开,会上透露,在今年的8-9月,有关管理部门将公布对没有通过品种的处置方案,积极调整相关审评资源、协调检查检验资源,研究完善相关评价要求和指导原则,分类推进289品种的评价,及时公告通过评价的品种。“289品种”未来命运如何?我们拭目以待!
责任编辑:露儿
-
一批药被查 涉维C银翘片、阿胶…
一批药被查 涉维C银翘片、阿胶…...
-
高值耗材最高降价80% 涉雅培、波科、贝朗…
8月1日,云南省曲靖市举行高值医用耗材联盟带量集中采购第一批次中选产品企业签约仪式。...
-
国家指令 整治所有医院回扣 暗访组出发
日前,国家卫健委发布了《2020年医疗行业作风建设工作专项行动方案》,这次方案的重点就是规范医疗机构及其从业人员行为,印发给各省、自治区、直辖市及新疆生产建设兵团卫生健康委,开始组织实施。...
-
医药代表系统学习产品知识的十个步骤
每个刚入行的医药代表初期都会接受公司大量培训,产品知识培训更是重中之重,不仅培训而且还要考试。...
-
“3+6”医用耗材带量采购,价格信息公布
吉林省政府采购中心消息发布《京津冀及黑吉辽蒙晋鲁医用耗材(人工晶体类)联合带量采购文件(LH-HD2020-1)》(下称《采购文件》),公布人工晶体类耗材的具体采购品种、申报价格等信息。 ...
-
首轮价格降幅低于42% 医疗器械企业直接淘汰
首轮价格降幅低于42% 医疗器械企业直接淘汰...
-
Q1最惨淡的两大药品领域,代表都离职了!
中国虽然是世界上最先控制住疫情的国家,但随着全球疫情的爆发,输入病例不断上升,加上中国本土还有不少无症状感染患者,这使得中国经济无法完全恢复正常。...
-
某些药企又要开启新一轮裁员了
做代表难,今年更加难。除了国家级的带量采购,省级也有带量采购,感觉就像是夹缝中求生存。...
-
两家外企大裁员,患教专员全部解散!
两家外企大裁员,患教专员全部解散!...
-
执业药师挂证,面临终生逐出行业的巨大风险
执业药师挂证,面临终生逐出行业的巨大风险...
-
虚开发票2.5亿,涉多家药械企业(附目录)
近日,国家税务总局马鞍山市税务局发布的《重大税收违法案件信息公告2020年3月》显示,51家企业涉嫌虚开发票,其中24家是药械企业或相关资讯、服务企业。...
-
91家药企收入公开:以岭、科伦、康恩贝…
突如其来的新冠肺炎疫情,对中国的冲击力和冲击面都超过了2003年的非典,对中国经济乃至世界经济也产生了不可避免的影响,也严重扰乱了正常的经济运行节奏。...





















