美国FDA如何监管OTC药品?

先普及一组小白级别的概念:
OTC(Over TheCounter):非处方药物,我国卫生部医政司是这样定义的:它是消费者可不经过医生处方,直接从药房或药店购买的药品,而且是不在医疗专业人员指导下就能安全使用的药品,即不需要凭借执业医师或助理医师的处方即可自行选购、使用的药品。
OTC在中国又分甲类OTC和乙类OTC。甲类(红色)的可在医院、药店销售;乙类(绿色)的是可以在医院、药店、超市、宾馆等地方销售。相对于OTC,RX是指必须凭借执业医师或医生开取的处方方可购买的药品,及处方药。

国内外OTC药品市场概况
OTC药品面对的是非常激烈的市场竞争,市场品牌是核心,优势企业集中度高。主要表现在:
品牌在 OTC 市场起到关键作用,因大多数OTC 药品没有专利保护,并且OTC 药品进入壁垒相对低,优势的企业能依靠品牌策略进行市场开拓。OTC 企业通过不断的提高品牌知名度产生市场效应,从而获得尽可能多的品牌溢价。
OTC 药品品牌往往能够决定药品的价格和销量。一般情况下,国家政策对于OTC 药品的价格管制少,企业主要根据市场状况进行自主定价,完全同质的药品可能由于知名度、药品包装的不同而形成显着的价格差异。
在全球市场,主要的OTC 药品企业包括强生、GSK、拜耳、诺华、赛诺菲安万特、惠氏、宝洁等。全球前十大知名药企的OTC 市场规模约占整体的34%,并有不断提升的趋势。
在中国,OTC 药物主要集中在感冒、止痛、消化领域。根据中国非处方药物学会的分类,我国 OTC 药物主要分为9 大类,包括感冒、胃肠、妇科炎症、止咳化痰、解热镇痛、皮肤外用、咽喉、维生素和其他。从领域看,感冒药、止痛药、消化道疾病治疗药品是当今全球OTC 药品市场的主导产品。
从消费者的医疗保健行为看,OTC 兼具保健品和处方药品的部分功能,存在三个交叉的市场,一部分市场与保健品形成竞争;一部分面对一些长期、慢性的细分疾病,具有较为固定的消费群体,与处方药争夺市场;最主要的市场则是面对自我药疗的常见疾病,如感冒、胃肠、皮肤炎症等。
美国是怎么逐步管理OTC药品的?
药品的监管是一个逐步认知的过程,FDA的成长过程让我们很清楚的看到了这一点。以下是FDA近60多年来法规进化过程,有兴趣的小伙伴可以详细去相关法案深入了解。
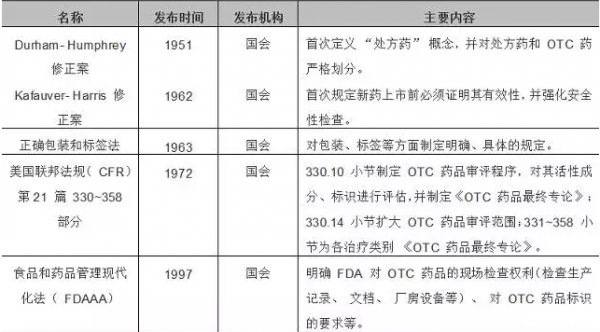
表1:美国与OTC 有关的主要法律法规
美国的OTC药品是怎么诞生的?
OTC药品有一套与处方药品完全不同的法规管理系统--“OTC专论”(OTC Monographs)。OTC专论是一种类似“食谱” 的资料,被编入《联邦管理法》。列入该专论系统的非处方药上市无须经过上市前标准审批流程。未列入OTC专论的药品上市途径主要有:
(1)上市前,向FDA递交申请,要求列入OTC专论;
(2)首先申请作为新处方药上市,销售多年后再申请转为OTC资格。
(3)值得一提的是,美国的OTC审评是一个公开的过程,任何人都可以提出申请,包括医药公司,医药专家,消费者或公众团体,药物资料信息采用公开征集的方式,任何持有相关资料的人员或机构都可以提交发表的或未发表的信息,最大限度的获取该类别药物全方位信息,专家审评组提交审议的结论和建议,相应内容将公布于众,多次举行听证会。
责任编辑:露儿
-
医院新规:查医药代表 挂钩产品
大医院严查医械代表再升级!私下接触医务人员,直接停止采购公司代理产品。...
-
编外人员被收保证金?医院取消编制大势所趋
看到一家县级医院向编外人员收取5000元工作保证金,限时不交清者,医院不再使用,老徐认为:编制制度或早已不适应医院发展需要了。...
-
三甲医院:8个药询价 要求至少稳定供货半年
三甲医院:供货不稳定,踢出一年。...
-
5省497名执业药师挂证被查实
今年“3•15”后,执业药师“挂证”问题引起全社会关注,按照国家药监局要求,自2019年5月1日起,各省级局组织对行政区域内的药品零售企业开展监督检查。...
-
又一大药陷入致癌风波 多家外企全球召回产品!
一些雷尼替丁药物又被查实含有NDMA杂质,目前山德士、葛兰素史克、印度瑞迪博士药厂均已停止雷尼替丁的供应并召回!...
-
大洗牌!国务院检查组,进入医疗器械企业了
国家严惩在医疗器械购买、销售、纳税...等多个环节的违规情况。...
-
4+7全国扩围,中标结果流出
大跌眼镜!4+7全国扩围结果出炉,有外企低价入围,部分原中选药企落标,多个品种再次刷新底价!...
-
国务院发文:医械行业,筛选重点企业监管
当监管方式越来越科学,不合规或打擦边球的械企面临的压力就越来越大。...
-
报告显示:多数医生不再愿意接待医药代表
报告显示,医生不再愿意接待医药代表,医药代表的必要性在降低。...
-
750家医药企业,最新离职率公布
2019年1月到6月的市场薪酬数据白名单公布,其中医药行业的行业增长和薪酬增长都维持稳定的高位;此外,报告采集了750家医药公司的数据,医药人的平均离职率仅为5.91%,为所有行业中最低的。...
-
63个药,底价曝光(附名单)
(9月6日),山东省药品集中采购网发布《关于山东省药品集中采购拟备案采购产品最低外省及拟挂网价格公示的通知》(以下简称《通知》)。...
-
医药业平均月薪公布 仍是最好的就业去向之一
据东方财富Choice数据,医药行业平均月薪为1.03万,同比涨幅较大,为11.75%,仅次于公用事业等行业,排名第六名。...





















